Cytek Biosciences品牌商
7 年
手机商铺
- NaN
- 0
- 1
- 2
- 1
推荐产品
公司新闻/正文
全光谱流式携手单细胞测序,揭开嗜酸性粒细胞神秘面纱
1614 人阅读发布时间:2023-11-10 10:01
研究背景
嗜酸性粒细胞是含有嗜酸性颗粒的一类白细胞,主要分布在胸腺、子宫、肺部、脂肪组织和胃肠道中,与过敏性气道炎症、特应性皮炎、嗜酸性食管炎和炎症性肠病等炎性疾病息息相关。其中,胃肠道中的嗜酸性粒细胞维持着宿主免疫反应的动态平衡,但其在肠道炎症反应中具体发挥的功能目前还不清楚。这篇发表在《Nature》杂志的文章突破了目前的技术瓶颈,将单细胞测序、全光谱流式和空间定位技术相结合,首次全方位描绘了嗜酸性粒细胞从骨髓到组织的发育图谱,揭示了肠道炎症反应中嗜酸性粒细胞扮演的角色。
研究方法
从5只B6J野生型小鼠中分离血液、脾脏、胃、小肠、结肠等标本,4℃染色50min后在5激光Cytek®Aurora全光谱流式上机检测,多参数结果采用UMAP降维和FlowSOM聚类分析。
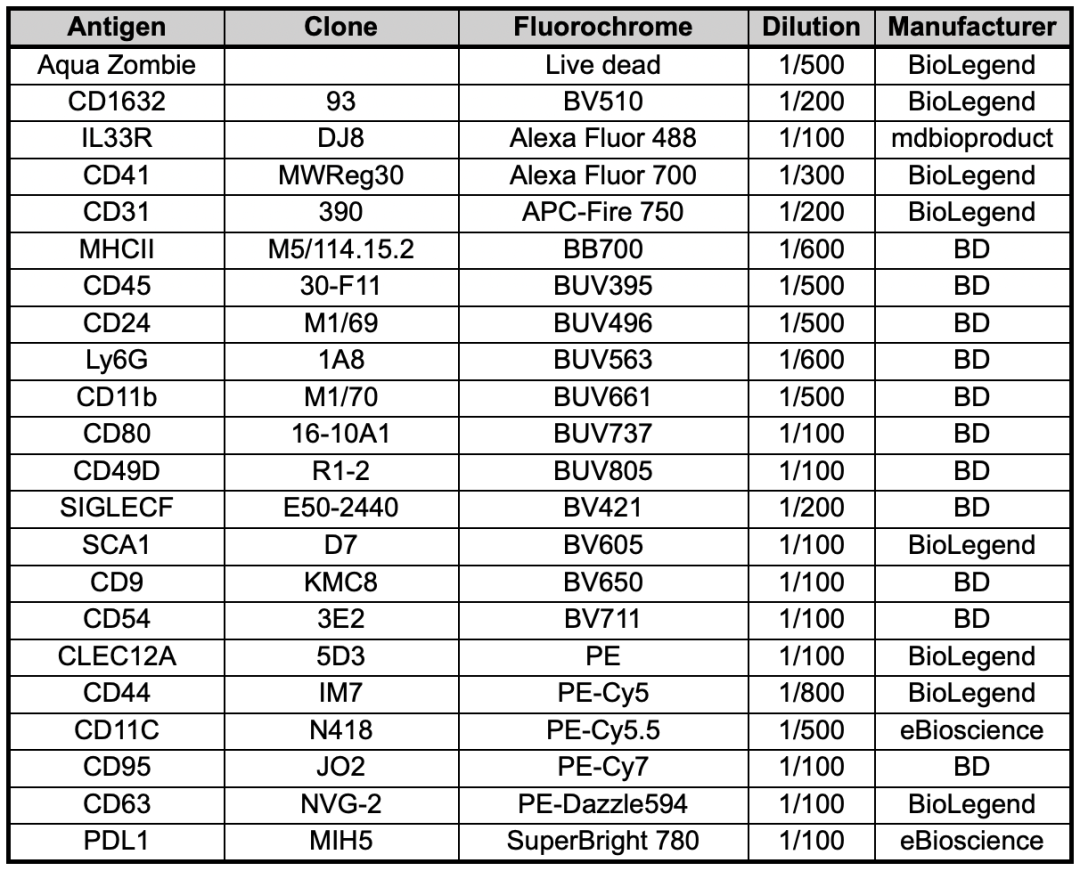
全光谱流式22色方案表征嗜酸性粒细胞
研究结果
胃肠道嗜酸性粒细胞主要分为A-Eos和B-Eos两个亚群
具有高丰度嗜酸性粒细胞的Il5-tg小鼠的骨髓、血液、脾脏、胃、小肠和结肠等组织样本的单细胞转录组测序结果显示,UMAP分析自动聚类为5个亚群,分别代表了不同的细胞发育阶段。其中,骨髓中主要是前体和不成熟的嗜酸性粒细胞,血液中主要是循环嗜酸性粒细胞。胃肠道中则主要是活跃(A)和基础(B)的两类嗜酸性粒细胞亚群,并且A-Eos被发现只存在于胃肠道中。A-Eos表达共刺激分子Cd80和Cd274(PD-L1),证明A-Eos参与了免疫调节的过程。因此,后续研究人员主要聚焦在这一群细胞上。利用全光谱流式Aurora剖析了野生型小鼠B6J血液、小肠和结肠等组织来源的单细胞样本的蛋白组数据,发现了A-Eos的特异性指标PD-L1和CD80。跟B-Eos相比,A-Eos表现出更强的细胞分泌活性(CD63, CD9, CD107)、颗粒度(SSC-A)和活化能力(Siglec-F)。从结肠粘膜的空间定位结果来看,A-Eos主要定位在管腔末端,B-Eos主要定位在粘膜下层,说明二者作用于不同的细胞微环境。研究人员进一步在人的肠道组织中也发现A-Eos和B-Eos与在小鼠组织中相似的空间定位,并且在炎症性肠病患者中A-Eos丰度显著提高,也提示A-Eos可能在肠道炎症反应中发挥作用。

胃肠道驻留的嗜酸性粒细胞转录组、蛋白组和空间定位结果
A-Eos发挥抗菌和免疫调节功能
研究人员在三个胃肠道炎症实验模型中同样观察到PD-L1+CD80+A-Eos比例显著增高,细菌感染后引起组织中循环嗜酸性粒细胞累积,血液和骨髓中不成熟嗜酸性粒细胞扩增。在体外与结肠培养上清(CM)共孵育后,骨髓、血液、脾脏来源的嗜酸性粒细胞都会分化为A-Eos,在体内也观察到脾脏来源的嗜酸性粒细胞(B-Eos)迁移到结肠后分化为A-Eos。沿着骨髓-血液-结肠的轨迹追踪,发现细菌感染引起循环和结肠A-Eos的粒细胞生成基因和抗菌基因的持续性表达。结肠来源的嗜酸性粒细胞和与CM孵育后的BM-Eos,分别同生物发光的细菌共培养之后,均表现出显著的杀菌能力。以上结论证明了A-Eos是具备抗菌和细胞毒性的一类特殊的嗜酸性粒细胞。此外,A-Eos上调包括IFNγ信号与MHC-I限制性抗原加工和呈递等免疫调节相关的基因,进而下调CD4+T细胞的增殖,说明A-Eos通过削弱CD4+T细胞反应从而减缓炎症的发生。

A-Eos展现抗菌和免疫调节双重功能
炎性肠病患者中A-Eos与CD4+T细胞共定位
研究人员进一步探索了发生炎症反应时A-Eos累积的上游调控机制,利用CRISPR抑制筛选和功能评估,发现细菌感染机体后,激活IL-33和IFN-γ信号通路,协同诱导炎症部位A-Eos的分化成熟。多重原位RNA成像结果显示,溃疡性结肠炎患者的结肠中CD4与SIGLEC8转录组存在共定位,证明了嗜酸性粒细胞和CD4+T细胞在空间位置上有接触。CD4相邻的SIGLEC8 RNA分子与A-Eos的分子CD80紧密相关,进一步证明了CD4+T细胞与A-Eos存在相互作用。
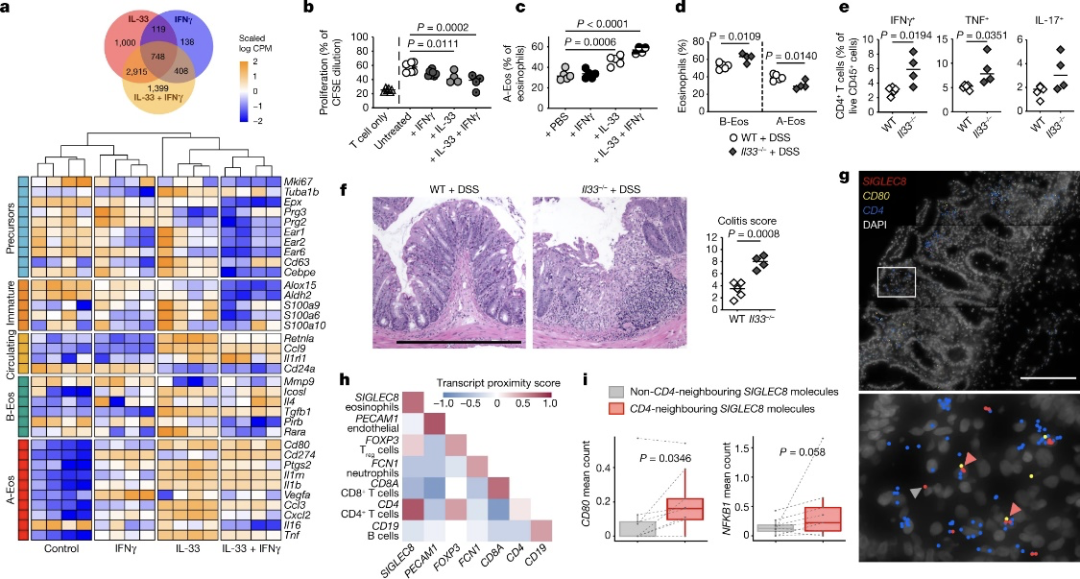
炎性肠病患者中A-Eos与CD4+T细胞相互作用
结 论
在肠炎治疗策略中,嗜酸性粒细胞一直是被忽视的对象,但在这篇文章中,研究人员开创性地表征了胃肠道疾病中嗜酸性粒细胞的多组学图谱,让我们看到了这一类细胞在炎性肠病治疗中的巨大潜力。细菌感染机体后,在胃肠道驻留的A-Eos能够起到抗菌和免疫调节的作用,抑制CD4+T细胞过度活化,从而减缓炎症负担,恢复宿主肠道微环境的稳态,这项研究为人类胃肠道疾病的靶向治疗提供了新的思路。
参考文献
Gurtner, A. et al. Active eosinophils regulate host defence and immune responses in colitis. 615, 151-157, doi:10.1038/s41586-022-05628-7 (2023).






