Cytek Biosciences品牌商
7 年
手机商铺
- NaN
- 0
- 1
- 2
- 1
推荐产品
公司新闻/正文
迎接曙光,全光谱流式分选仪助力中国科学家突破肝癌免疫治疗瓶颈
181 人阅读发布时间:2026-01-15 12:27
亮点一览
免疫检查点抑制剂疗法作为肿瘤免疫治疗的革命性突破,在临床应用中呈现出广阔的发展前景,然而,其在肝癌治疗中响应率却并不高。有研究表明,肿瘤相关的巨噬细胞(TAM)在肿瘤微环境中往往扮演着“帮凶”的角色,肿瘤免疫逃逸与治疗效果不佳都与之息息相关。来自杭州医学院的徐骁/王建国团队发现,CX3CR1+ TAMs在肝癌治疗中“使绊子”,通过分泌IL27阻碍CD8+ T细胞“前线杀敌”。靶向CX3CR1+ TAMs和抗PD1疗法“双管齐下”,能够显著改善肝癌临床治疗的效果1。
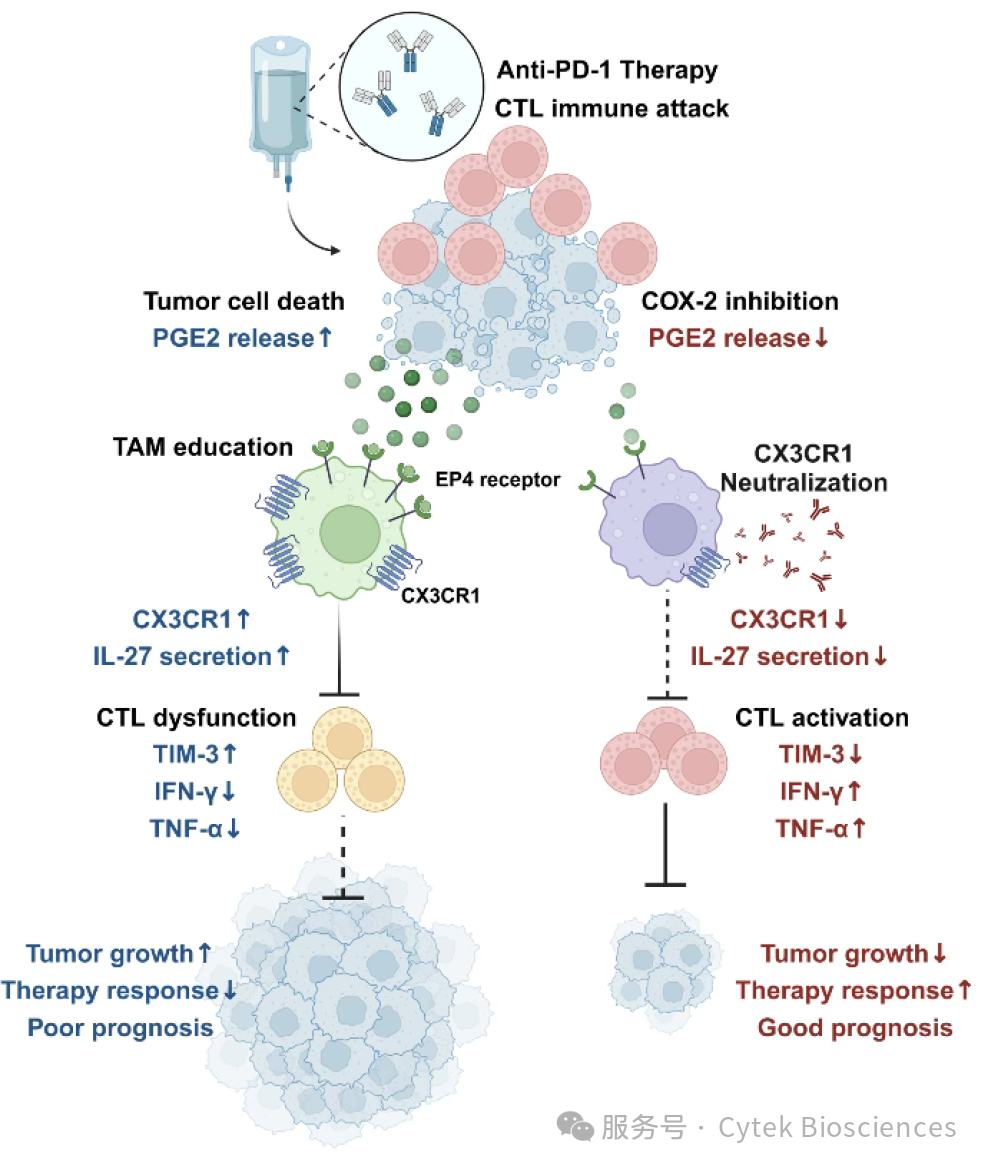
图1 – 靶向TAMs增强抗PD1肝癌治疗概览图
肿瘤免疫治疗回顾
在肝癌治疗中,传统疗法收效甚微,而免疫疗法则受到越多越多的关注,通过调动宿主免疫系统主动去攻击肿瘤,为临床治疗打开了全新的思路。免疫疗法主要分为免疫检查点抑制剂疗法(ICI)、过继性细胞治疗(ACT)和肿瘤疫苗等,其中,免疫检查点抑制剂疗法在多种肿瘤治疗中疗效显著。尽管如此,ICIs在肝癌治疗中响应率一直不高,成为临床治疗中一大急需攻关的课题。在多种肿瘤的免疫微环境中常常能发现CX3CR1+ TAMs的身影,但是肝癌与TAMs的关系却依旧是一个未解之谜。
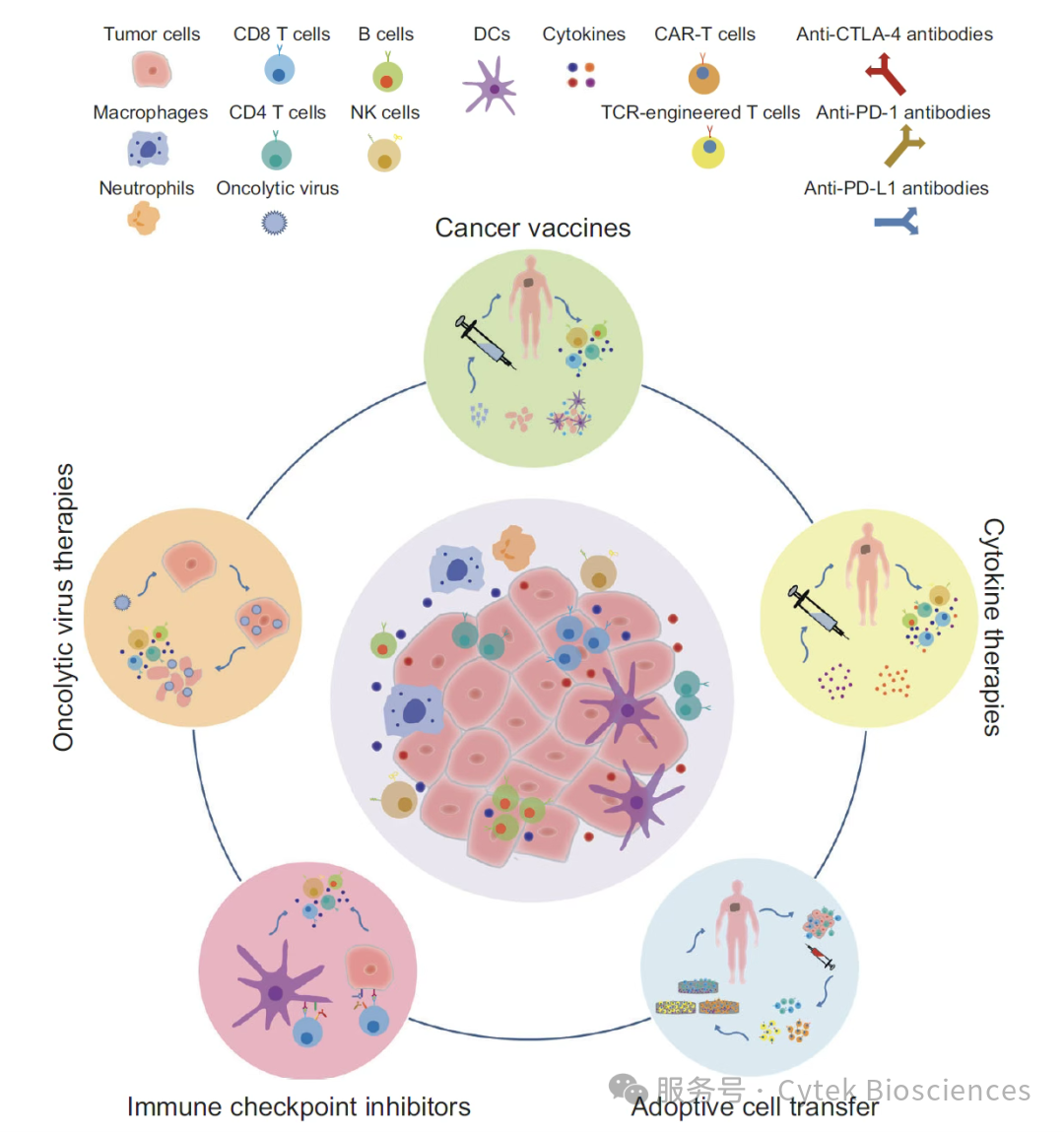
图2 – 肿瘤免疫疗法示意图2
全光谱流式分选仪
让TAMs无处遁形
研究人员收集小鼠肿瘤,去除坏死组织、血凝块和邻近的正常组织后,处理成单细胞悬液。流式分析结果发现抗PD1处理的实验组中,肿瘤浸润的TAMs比例增加(图3A),并且CX3CR1表达丰度增加(图3F)。利用Cytek® Aurora™ CS全光谱流式分选仪识别并分选肿瘤浸润的CD45+ 免疫细胞(图3H-J)以及CD45+ CD11b+ F4/80+ CX3CR1+ TAMs(图3K),并对接单细胞测序平台,结果呈现出CX3CR1+ TAMs活跃的代谢特征和细胞因子分泌能力,这可能与适应性免疫反应相关。
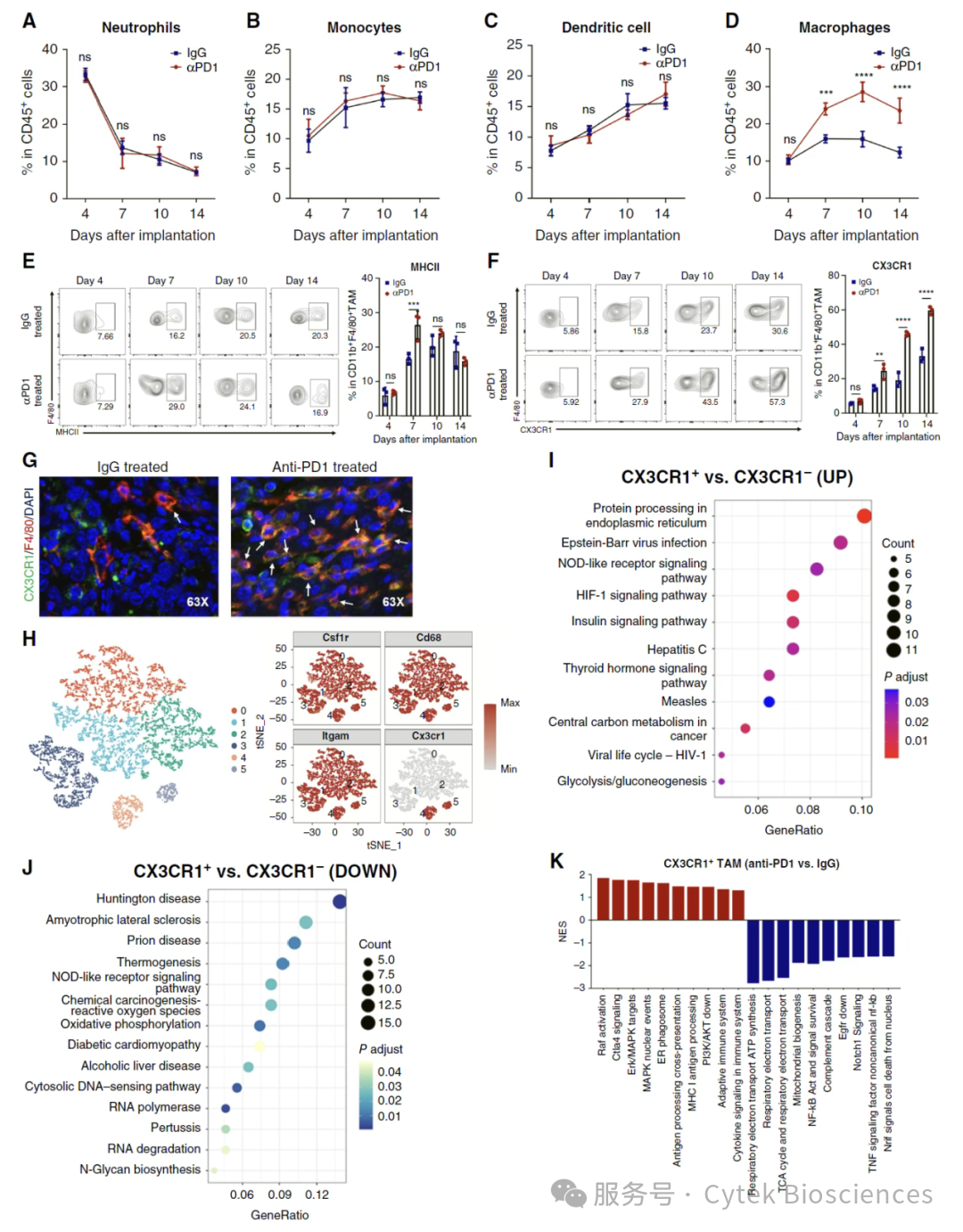
图3 – 分选肿瘤浸润的免疫细胞
并对接单细胞测序平台
CX3CR1+ TAMs如何对于
抗PD1疗法 “从中作梗”?
为了探究CX3CR1+ TAMs在抗PD1疗法中的调控机制,利用Cytek Aurora CS全光谱流式分选仪从PD1抗体处理过的小鼠的肿瘤样品中分选出CX3CR1+ 和CX3CR1- TAMs,发现CX3CR1+ TAMs细胞的培养上清大量分泌IL27。当CX3CR1+ TAMs与CD8+ T细胞共培养时,CD8+ T细胞表达TIM3上调,与此同时,TNFα与IFNγ表达下调。这一现象在加入IL27重组蛋白(rmIL27)时同样能够观察到,而加入IL27抗体(antiIL27)则阻断了这一过程,证明了CX3CR1+ TAMs通过分泌IL27诱导CD8+ T细胞发生耗竭。
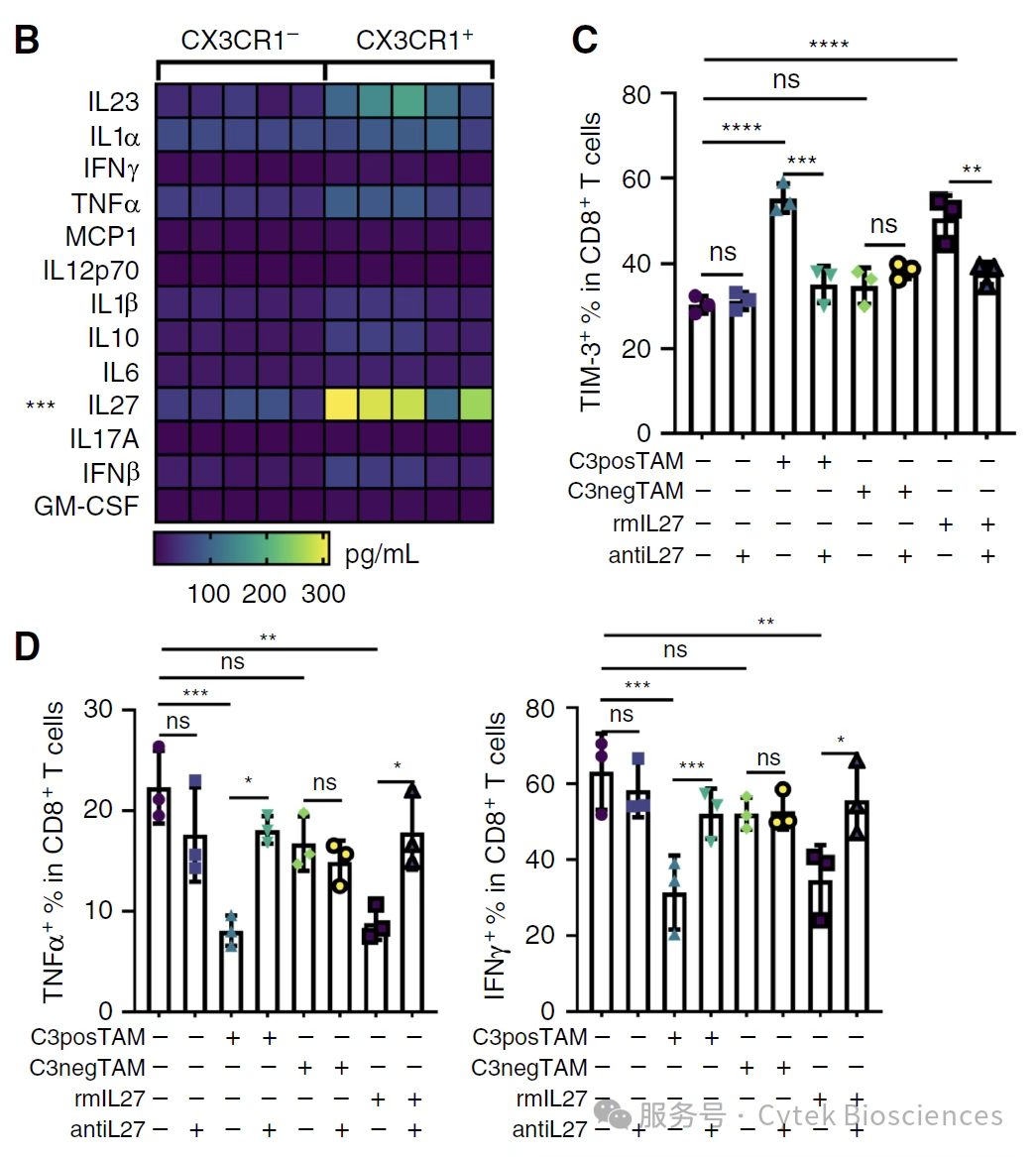
图4 – CX3CR1+ TAMs分泌IL27诱导CD8+ T细胞耗竭
总结展望
免疫检查点抑制剂疗法在肿瘤免疫治疗领域成效卓著,而针对响应率不高的肝癌治疗,本研究另辟蹊径,从肿瘤“帮凶”TAMs着手,通过靶向CX3CR1+ TAMs联合抗PD1疗法,重塑CD8+ T细胞功能,为肝癌临床治疗带来新的曙光。
Cytek Aurora CS全光谱流式分选仪在高维方案分选中展现出无可比拟的显著性优势,在本研究中,面对相对简单的流式方案,也同样呈现了卓越的分选性能,从肿瘤样品中精准识别分选到目的细胞,并对接下游单细胞测序或免疫细胞共培养实验,展现出高纯度、高活性的高性能分选结果。展望未来,面对珍贵的肿瘤患者临床样本,全光谱流式分选仪的无限潜能有望推动该领域研究取得更多突破性成果。当极光划破夜幕,曙光便悄然降临。
注:本文主要解读了原文中围绕全光谱流式分选仪开展的部分结果,更多细节,请阅读原文获取。
参考文献
1.Xiang, X. et al. Blocking CX3CR1+ Tumor-associated Macrophages Enhances the Efficacy of Anti-PD1 Therapy in Hepatocellular Carcinoma. Cancer immunology research, doi:10.1158/2326-6066.CIR-23-0627 (2024).
2.Zhang, Y. & Zhang, Z. The history and advances in cancer immunotherapy: understanding the characteristics of tumor-infiltrating immune cells and their therapeutic implications. Cellular & molecular immunology 17, 807-821, doi:10.1038/s41423-020-0488-6 (2020).






