Cytek Biosciences品牌商
7 年
手机商铺
- NaN
- 0
- 1
- 2
- 1
推荐产品
公司新闻/正文
Nature上新!反其道而行,Amnis®成像流式细胞术助力揭示肿瘤反应性CD8⁺ T细胞生物学特征及应用价值
318 人阅读发布时间:2026-04-05 23:08
在流式细胞术分析分选以及单细胞测序实验中,排除细胞聚集体,聚焦单细胞是常规操作。而在荷兰癌症研究所的研究者发表于《Nature》杂志的研究中颠覆了这一常规思路,研究者反其道而行之,将目光投向那些在分析中被排除的细胞聚集体。借助Cytek® Amnis® ImageStream®X成像流式等技术,在黑色素瘤临床样本中直观证实了由CD8⁺ T细胞与肿瘤细胞和/或抗原呈递细胞(APC)形成的异型簇的存在。研究揭示,这些曾被忽略的细胞簇恰恰富集了具有强大肿瘤杀伤活性的T细胞,展现出巨大的基础研究价值与临床应用潜力。

人T细胞与肿瘤细胞间形成异型细胞簇
为研究人T细胞与肿瘤细胞的功能性相互作用,通过基因工程改造黑色素瘤细胞,使其同时表达HLA-A*02:01分子、MART-1肿瘤抗原及mPlum荧光标记,并转导MART-1特异性T细胞受体(TCR)到源于健康供体的CD8+T细胞,并用CellTrace Violet(CTV)进行标记,共培养上述的肿瘤细胞和T细胞后,使用Amnis®成像流式系统直观检测到了肿瘤细胞和T细胞之间形成了细胞簇(如图1)。
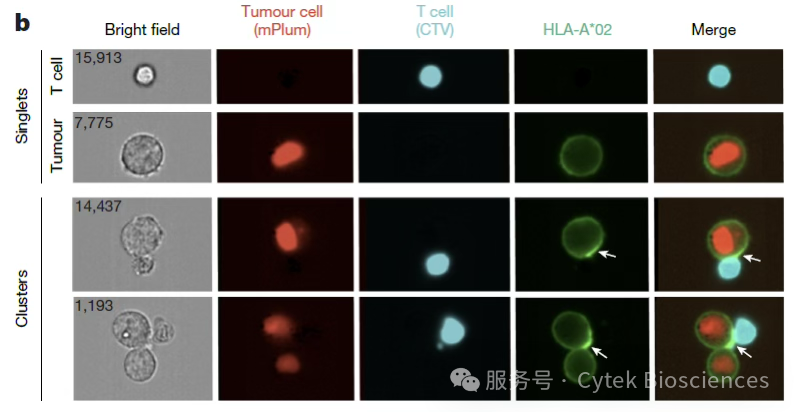
图1:黑色素瘤细胞与T细胞共培养4小时后,
经染色后通过Amnis®成像流式细胞仪进行检测
并且从图片中直观观察到HLA-A*02、ICAM1和CD58特异性重定位至T细胞-肿瘤细胞接触界面,说明肿瘤细胞和T细胞之间形成了免疫突触(图2)。除了黑色素瘤,在非小细胞肺癌、前列腺癌、结肠癌和乳腺癌等多种癌症中也发现了这种现象。
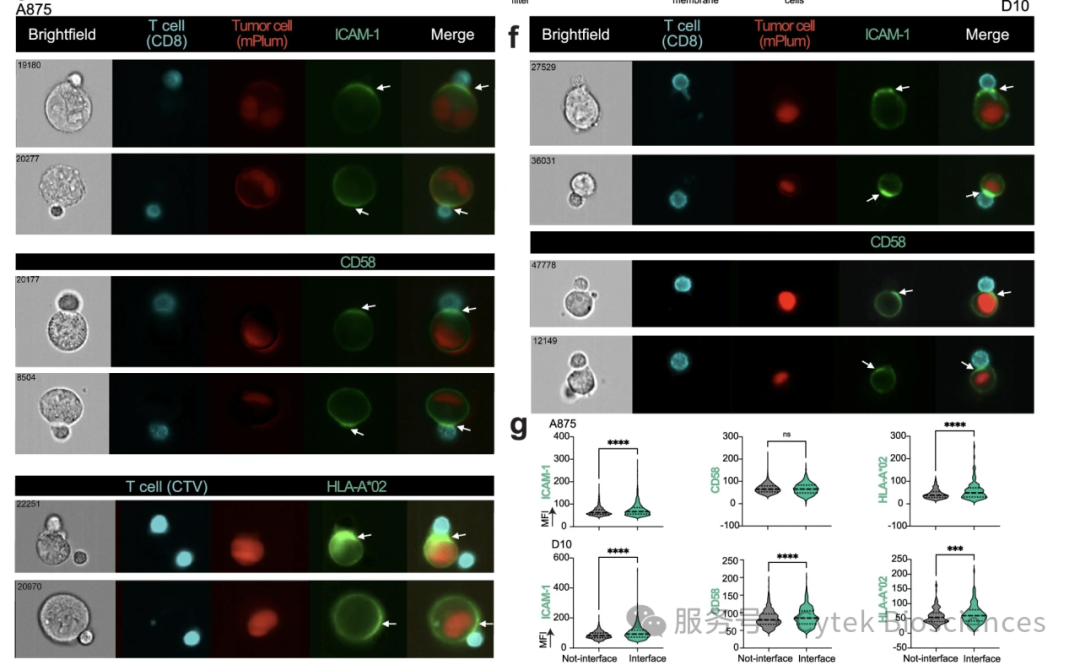
图2:肿瘤细胞和T细胞之间形成了免疫突触
抗原特异性T细胞的竞争性
进一步,将非特异性T细胞与MART-1特异性T细胞混合,使两者竞争与肿瘤细胞结合,为模拟肿瘤微环境中肿瘤反应性T细胞占比低的生理状态,进行梯度稀释实验,结果表明即使特异性T细胞仅占T细胞总数的1%,其在肿瘤细胞簇中的富集度仍可达11倍(图3f),并且该竞争优势在多种癌症类型中均得到验证(图3g)。
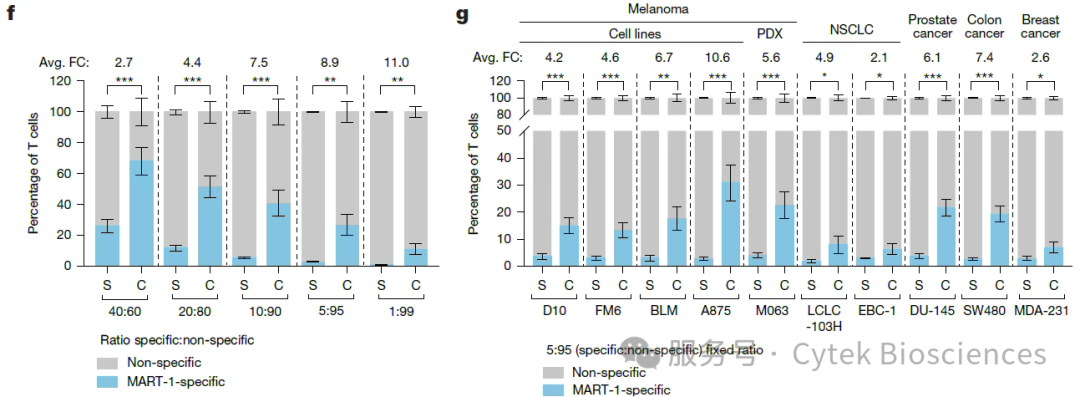
图3:f)将A875黑色素瘤细胞与不同比例的MART-1特异性T细胞
与非特异性T细胞混合物共培养4小时;
g)将不同癌细胞系与比例为5:95的MART-1特异性T细胞
与非特异性T细胞混合物进行共培养
为评估不同T细胞群体的肿瘤杀伤能力,采用快速扩增方案(REP)培养单体型或簇源性T细胞,在负载人黑色素瘤的免疫缺陷NSG小鼠中进行两轮过继细胞转移(ACT)(图4h)。结果显示,扩增的单体型T细胞无肿瘤控制效果,而源自异型簇的T细胞可显著抑制肿瘤生长(图4i)。
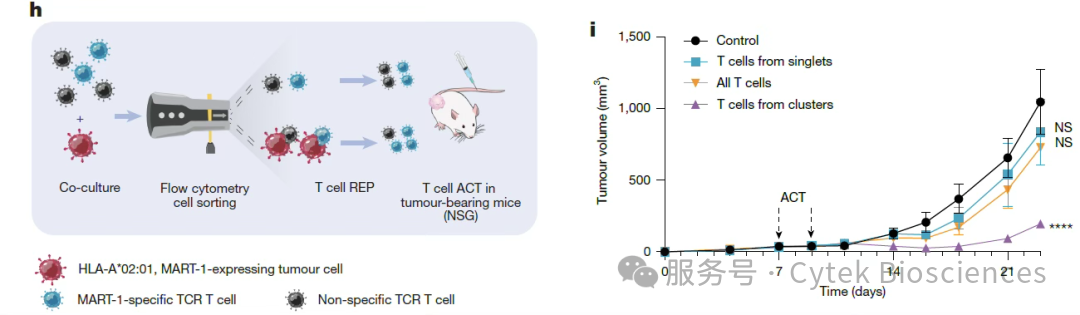
图4:h)体内实验示意图;
i)过继细胞转移后肿瘤的生长曲线
临床异型CD8+T细胞簇的研究
基于上述的研究发现,研究者想进一步探索CD8+T细胞与肿瘤细胞之间形成的异型簇是否也能直接从临床癌症样本中分离,为此分析了21例来自不同解剖部位的黑色素瘤样本,在所有患者样本中观察到了异型CD8+ T细胞-黑色素瘤细胞簇以及CD8+T细胞-APC簇。
使用Amnis®成像流式进一步直观确认这些异型细胞簇中包含肿瘤细胞-T细胞簇、APC-T细胞簇以及肿瘤细胞- APC细胞-T细胞簇(图5)。免疫突触标志物CD11c、HLA-ABC和CD58显著重定位至细胞-细胞接触界面(图5)。
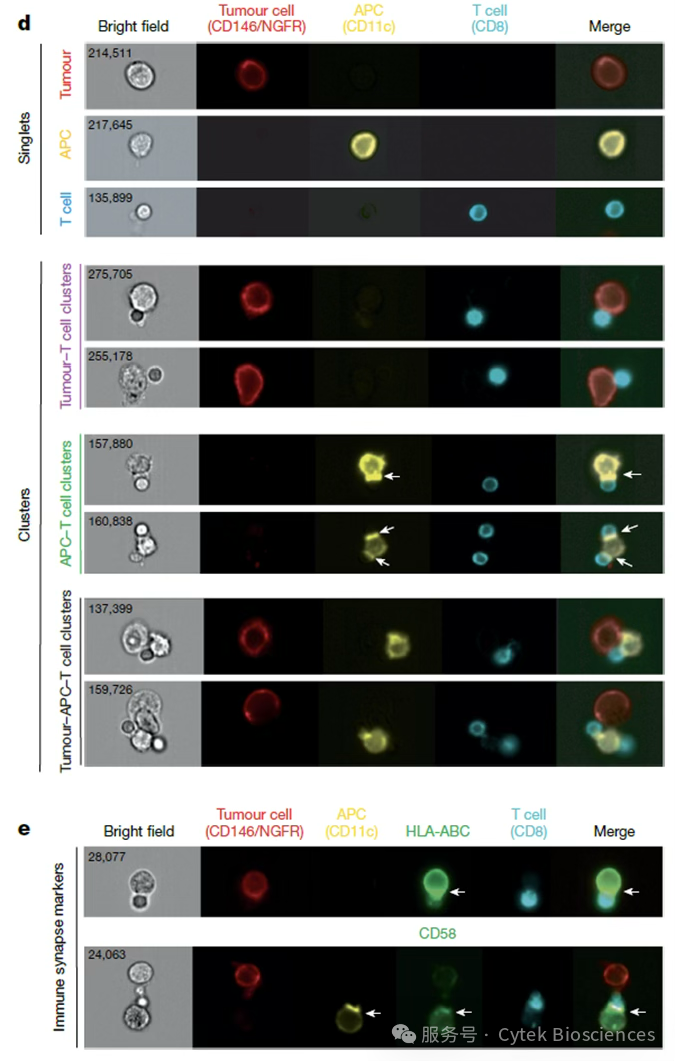
图5:使用Amnis®成像流式检测肿瘤患者样本中的
异型细胞簇及形成的免疫突触
同时还鉴定出包含CD4+ T细胞、肿瘤细胞和APCs的簇结构(图6)。
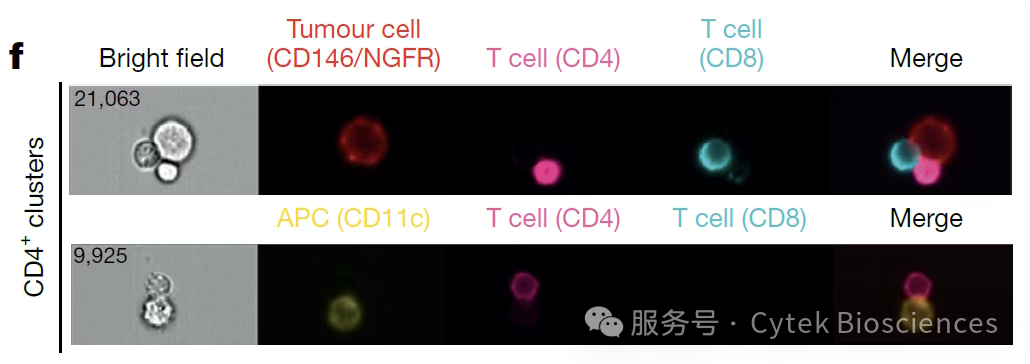
图6:使用Amnis®成像流式检测包含CD4⁺ T细胞的代表性异型簇
测序和功能分析
为深入比较单体型与细胞簇中CD8⁺ T细胞、肿瘤细胞及APC的差异,研究者采用单细胞RNA与TCR测序技术进行分析。结果显示,相较于单体T细胞,簇源CD8⁺ T细胞表现出更显著的耗竭表型、更强的肿瘤反应性及更高的TCR克隆性,其独特的RNA谱对TIL治疗反应具有预测价值。
进一步分析发现,当TCR匹配的T细胞与APC结合时,相较于与肿瘤细胞结合,会表现出更强的耗竭与共调节特征。此外,对异形簇中细胞的分析表明,CD8⁺ T细胞倾向于优先与特定的APC及肿瘤细胞亚群结合,并通过特定配体-受体对进行通讯。
此外功能实验证实,簇源CD8⁺ T细胞在体外及体内均展现出显著优于单体CD8⁺ T细胞的抗肿瘤活性。
小结
本研究通过强大的Amnis®系统的多色成像流式技术,拓宽了常规流式细胞分析的视野,不仅成功捕获并证实了肿瘤微环境中长期被忽视的异型细胞簇的存在,还清晰呈现了异形簇中CD8⁺ T细胞和肿瘤细胞形成的免疫突触,用直观的证据证实了异形簇中的CD8⁺ T细胞的肿瘤杀伤功能。此外,Amnis®系统强大的定量统计功能,在短时间内对大量样本中的异型细胞簇及形成的免疫突触进行检测和定量统计,为研究结果提供精准有力的数据支撑。
这些富含肿瘤反应性CD8⁺ T细胞的细胞簇,不仅是一个具有独特生物学特征的细胞群体,更是解密肿瘤-免疫细胞功能性相互作用的关键窗口。该研究支持改进TIL疗法以及基于从簇状T细胞中分离TCR的治疗策略,具有极高的临床应用前景。
参考文献:
Ibáñez-Molero S, et al. Tumour-reactive heterotypic CD8 T cell clusters from clinical samples. Nature. 2026






