Cytek Biosciences品牌商
7 年
手机商铺
- NaN
- 0.5999999999999996
- 0.5999999999999996
- 1.5999999999999996
- 0.5999999999999996
推荐产品
公司新闻/正文
首次!全光谱流式分选仪联合单细胞测序仪为人类骨骼干细胞“画像”
33 人阅读发布时间:2026-04-05 23:09
什么是人类骨骼干细胞(hSSCs)
2018年,美国斯坦福大学医学院干细胞生物学与再生医学研究所Charles K.F. Chan团队第一次鉴定并分离到人类骨骼干细胞(hSSCs),这是一类存在于骨骼组织中,具备自我更新与多向分化潜能的干细胞,其主要参与的功能包括骨骼生长发育、维持骨骼稳态,骨骼损伤修复等。hSSCs功能异常是骨骼衰老与疾病的核心机制。
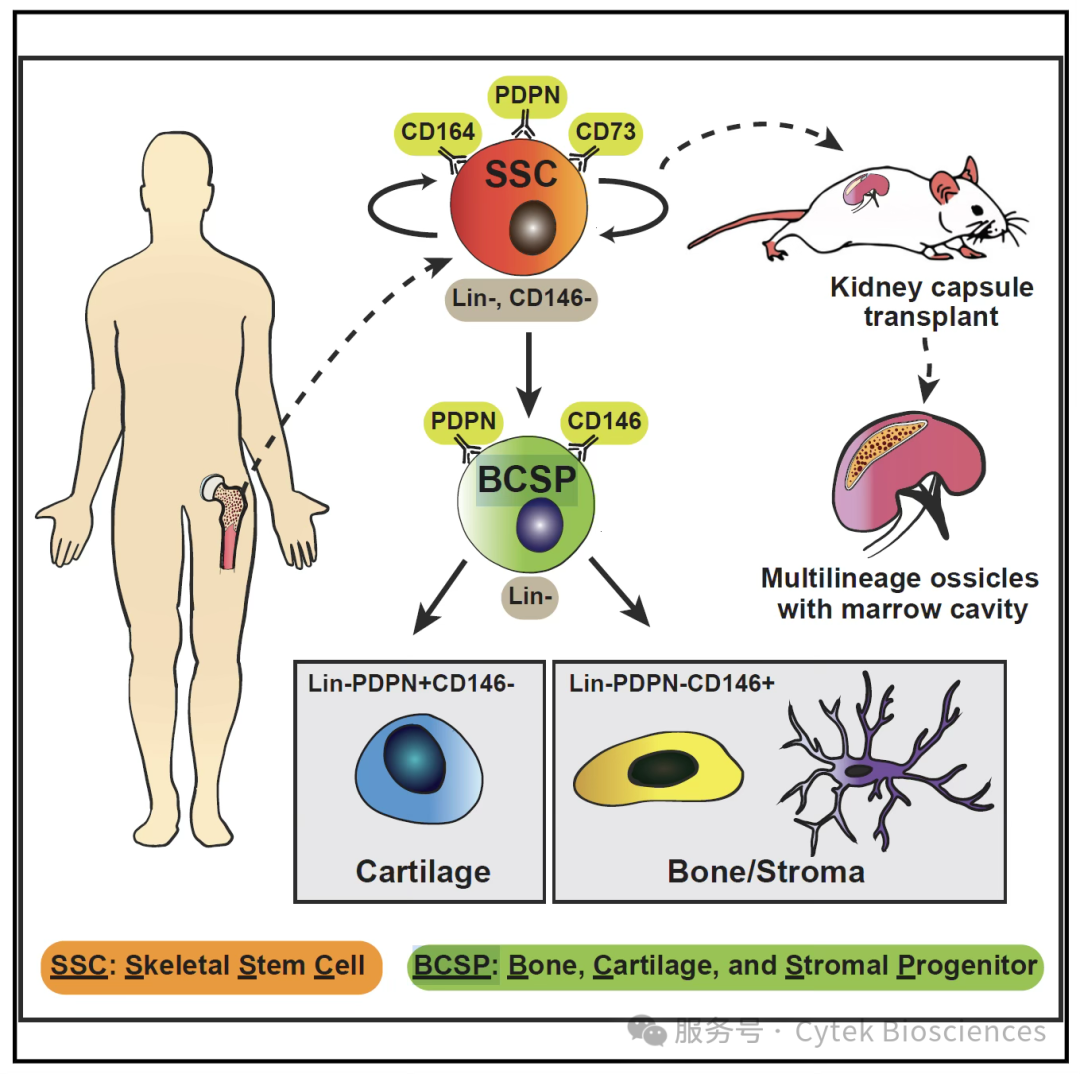
图1 – 首次鉴定并分离人类骨骼干细胞1
研究亮点
由于样本可及性的限制,目前对于人类骨骼干细胞的研究深度远远不及造血干细胞。继首次成功鉴定hSSCs之后,Charles K.F. Chan教授带领团队再一次在这一领域获得了突破性进展,第一次对10个胎儿骨骼位点的hSSCs、以及成年患者的hSSCs开展了系统性分析,完成了四种不同hSSCs亚型的分离、鉴定、定位和功能验证,并发现骨骼衰老与疾病的典型特征是纤维化hSSCs亚型占据主导地位,该团队的开创性成果发表于国际前沿学术期刊《Cell Stem Cell》(IF 20.4)。
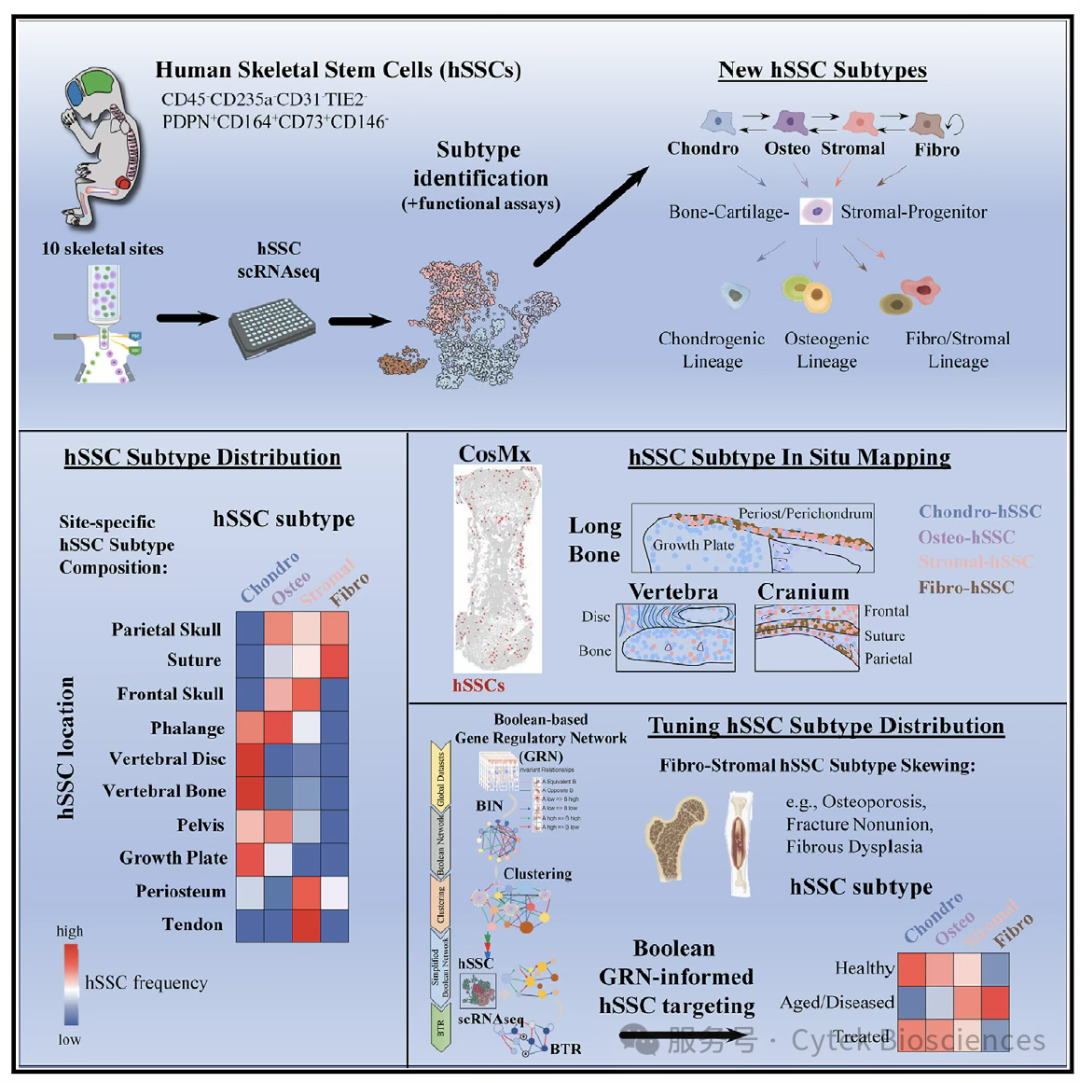
图2 - 第一次系统性描绘人类骨骼干细胞表型图谱2
Cytek® Aurora™ CS系统
释放全光谱流式分选应用潜能
1
PCR孔板分选,对接单细胞测序
选取胎龄为17至20周的人类胎儿的十个骨骼部位采样,基于Cytek® Aurora™ CS全光谱分选型流式细胞仪分选人骨骼干细胞(CD45-CD235a-TIE2-CD31-CD146-PDPN+CD73+CD164+)至96孔PCR板中,下游对接单细胞转录组测序(图3A)。10个采样点的hSSCs表现出显著的细胞异质性(图3B, C),通过标志物表达分析和通路富集分析对所有hSSCs进行无偏倚的Leiden聚类后发现,hSSCs可分为四种主要类型,分别对应软骨形成、成骨形成、基质形成及成纤维形成的基因表达模式(图3D, E)。
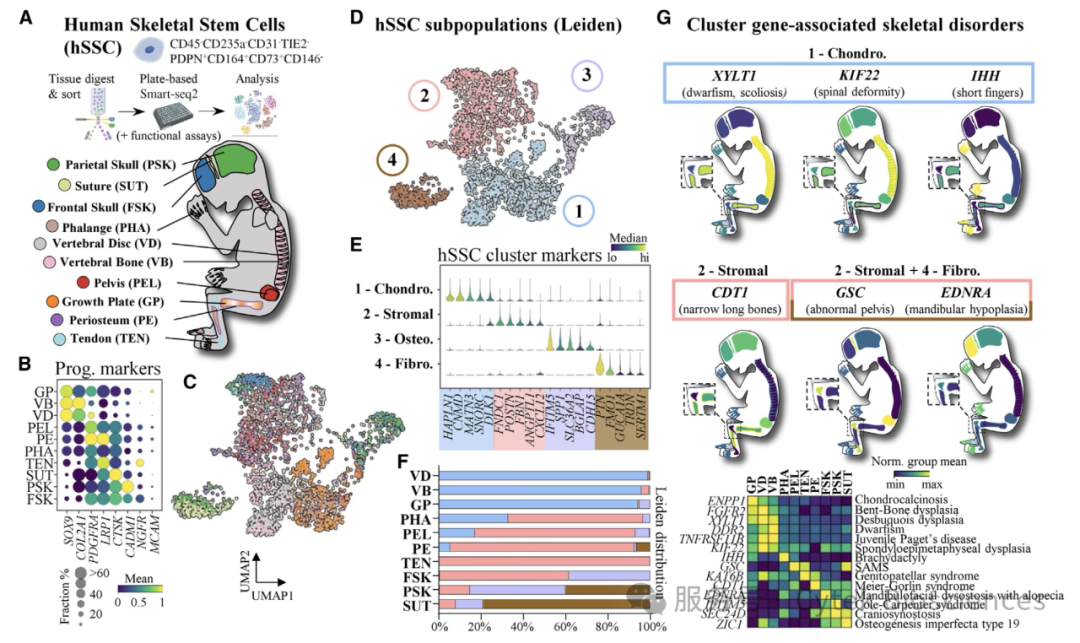
图3 – 分选并对接测序平台,鉴定hSSCs的异质性
2
索引分选,精细描绘hSSCs谱系树
为了更清晰地阐明hSSCs的成骨谱系分化过程,基于Cytek® Aurora™ CS全光谱分选型流式细胞仪分选生长板(Growth Plate,GP)的hSSCs及其已明确的祖细胞亚型(人骨软骨祖细胞hBCSPs与人成骨祖细胞hOPs),并对接单细胞测序平台(图4A-D)。采用Cytek® Aurora™ CS分选仪的索引分选功能,回溯分选到孔板中每个单细胞所对应的免疫表型,筛选出新的细胞标志物组合,利用该组合可以从hOPs群体中精准区分出hSSCs来源的成骨祖细胞亚群(OPC:PDPN⁻CD146⁺CD73⁻)和基质祖细胞亚群(SPC:PDPN-CD146hiCD73low)(图4E)。
如前文所述,基于单细胞测序结果鉴定出4种hSSCs类型,同样通过索引分选的方式,筛选了能够区分这4种hSSCs类型的细胞标志物组合CD73/CD164(图4G)。分别分选这四种hSSCs类型,并进行体内骨小体形成实验,证实了每种亚型均具备真正的骨骼干细胞特性,即自我更新能力和多向分化潜能(图4H, I)。
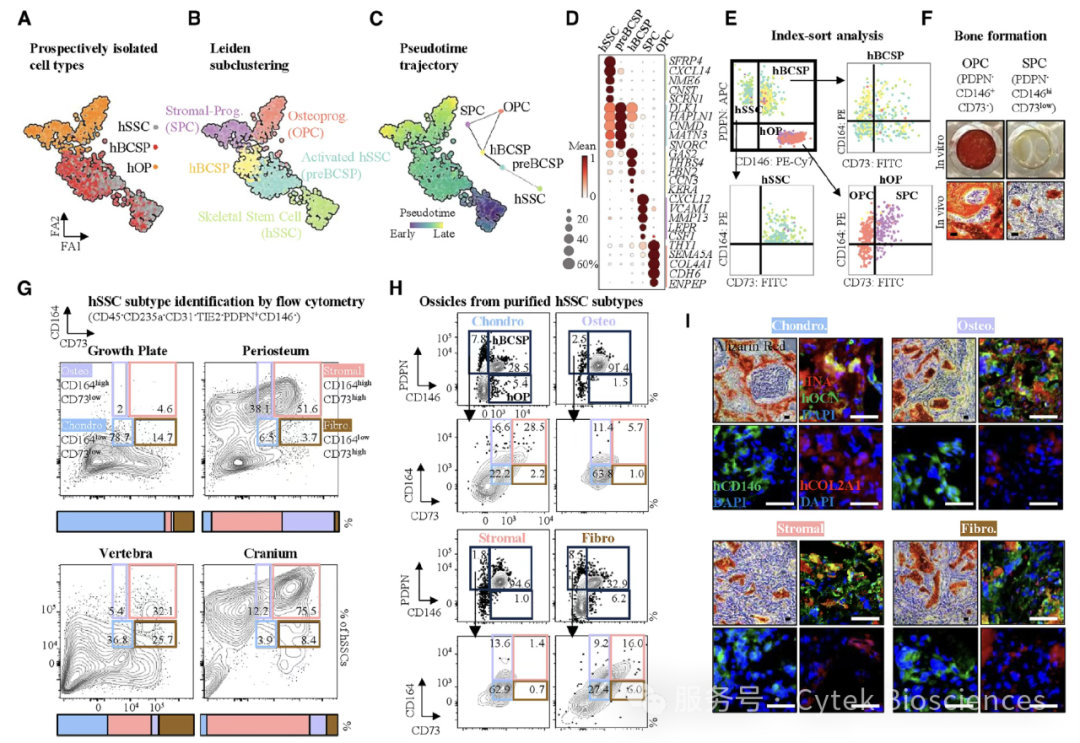
图4 – 索引分选结合测序分析,获得多组学结果
3
三次高活性分选, hSSCs克隆体内示踪
为了实现hSSCs的体内克隆追踪,研究人员使用Cytek® Aurora™ CS全光谱分选型流式细胞仪,分选了来自生长板(GP)与骨膜(PE)的hSSCs。随后转导慢病毒条形码文库(包含Venus报告基因),二次分选Venus+的hSSCs后,移植到受体小鼠的肾包膜中,3周后分离移植组织,又一次分选Venus+的hSSCs,进行单细胞测序分析,证明了生长板与骨膜来源的hSSCs之间存在显著的分化差异。
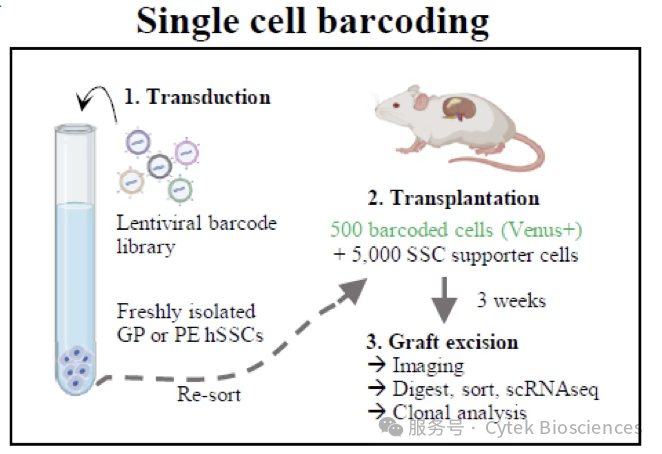
图5 – 人类骨骼干细胞的体内克隆条形码追踪实验
总结展望
研究团队开创性地分选及鉴定了四类hSSCs亚群,这标志着对人类骨骼干细胞的认识提升至新高度,也为制定针对骨骼衰老及相关疾病的有效干预策略提供了全新的视角。Cytek® Aurora™ CS全光谱分选型流式细胞仪极大地加速了研究进程,高活性、高纯度、高活性的卓越分选性能为高质量分选结果保驾护航;巧妙的倾斜式孔板适配器设计,保证了PCR孔板高精度分选;索引分选结合单细胞测序数据,拓展了单细胞多组学研究的分析维度及解析深度。极光分选,尽情释放全场景的分选应用潜能。
参考文献
1Chan, C. K. F. et al. Identification of the Human Skeletal Stem Cell. Cell 175, doi:10.1016/j.cell.2018.07.029 (2018).
2Ambrosi, T. H. et al. Human skeletal development and regeneration are shaped by functional diversity of stem cells across skeletal sites. Cell stem cell, doi:10.1016/j.stem.2025.02.013 (2025).






