Cytek Biosciences品牌商
7 年
手机商铺
- NaN
- 0
- 1
- 2
- 1
推荐产品
公司新闻/正文
揭开免疫突触奥秘:Amnis®成像流式助力TCR免疫疗法突破肿瘤治疗壁垒
405 人阅读发布时间:2025-09-04 14:51
KRAS基因突变(如G12V)是结直肠癌、胰腺癌和肺癌的关键驱动因素,但因缺乏可成药靶点,传统药物研发举步维艰。T细胞受体疗法(TCR engager)是一种新兴的免疫疗法,通过招募和重定向T细胞攻击肿瘤细胞。与CD3双特异性抗体相比,可溶性TCR engager能够靶向由MHC呈递的胞内和胞外抗原,具有更广泛的靶点覆盖范围,为实体瘤治疗带来新希望。然而,生理亲和力与脱靶毒性的平衡始终是瓶颈:
-
天然TCR亲和力(1–100 μM)不足,而人工增强易致交叉反应(如MAGE-A3疗法致死案例);
-
现有TCR衔接器(如Immunocore的ImmTAC)结构单一,且依赖高亲和力TCR(如Kimmtrak的80 pM),存在T细胞耗竭风险。
在此背景下,浙江大学医学院附属第二医院谭曙光研究员与中国科学院微生物研究所高福院士和深圳儿童医院谭回研究员团队合作,成功设计出一种高效的可溶性单链TCR engager(STanD-scTCR),显著增强了T细胞活性和肿瘤抑制效果,同时保持了生理亲和力并降低了脱靶风险。这项研究为TCR engager类药物的研发提供了新的思路和有价值的参考,具有临床转化潜力。
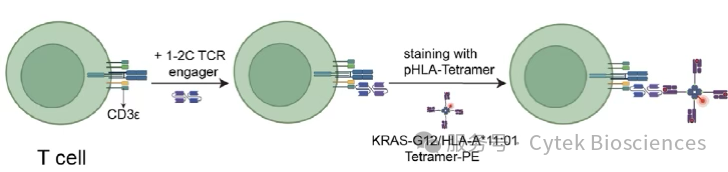
图1. 1–2C TCR 接合器与 T 细胞结合的检测示意图
双链结构与点突变协同:TCR engager优化新路径
1 创新结构设计 -- STanD-scTCR
-
构建串联双链scFv TCR(图2-1:1–2C-2LL),显著提升结合亲合力与稳定性(图22-2);
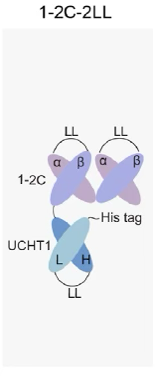
图2-1. 串联双链scFv TCR:1–2C-2LL
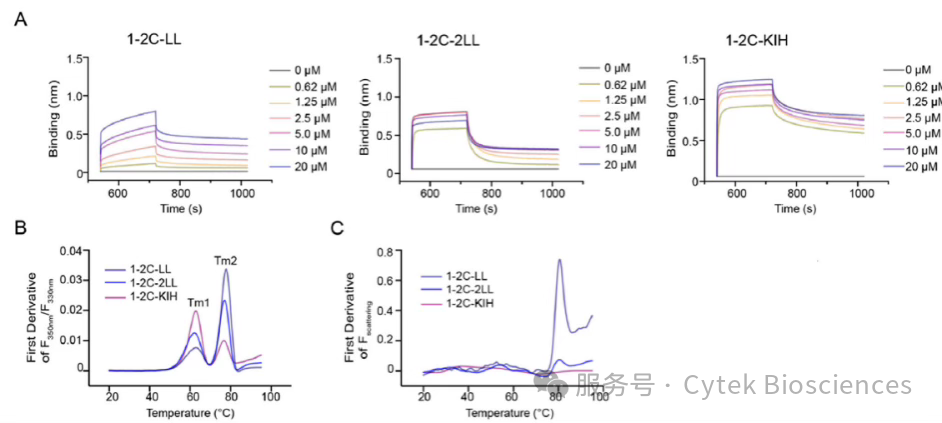
图2-2. TCR衔接器的结合特性、热稳定性
-
相比单链(1–2C-LL)和四聚体(1–2C-KIH)(图3-1),双链结构在保持特异性的同时,激活T细胞效能最佳(图3-2)。
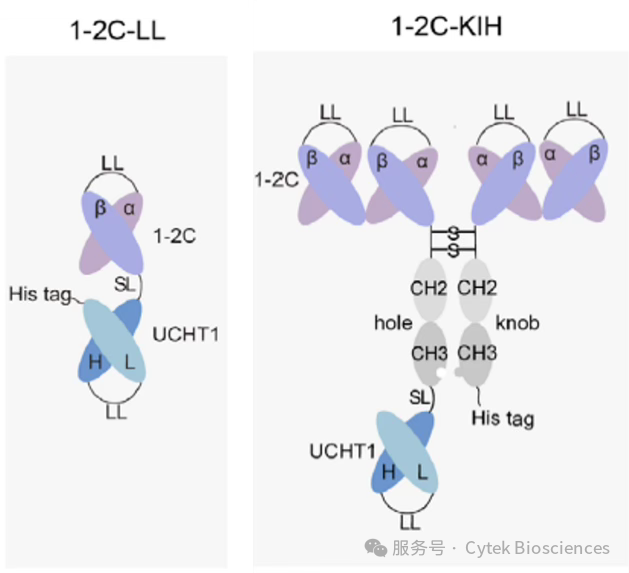
图3-1. 单链(1–2C-LL)和四聚体(1–2C-KIH)
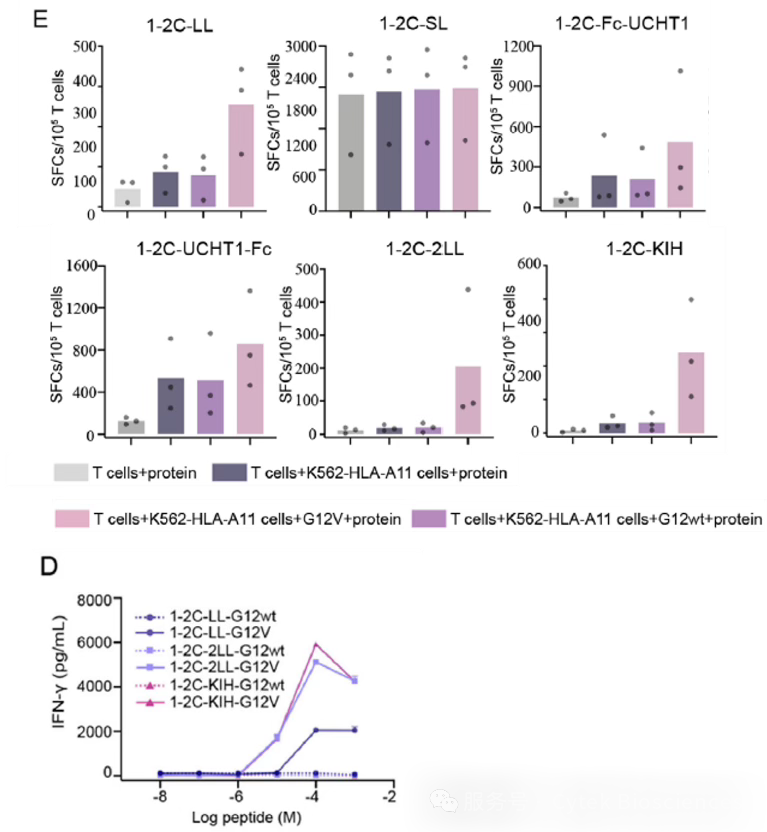
图3-2. 双链结构激活T细胞效能最佳
2 精准点突变 -- T96F优化
-
通过Rosetta ΔG模拟筛选出TCR β链T96F突变(图4);
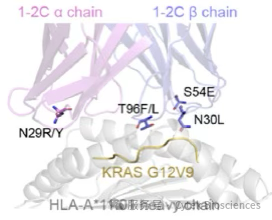
图4. 1–2C/KRAS-G12V/HLA-A11:01 复合体结构
-
维持生理亲和力(KD=2.88 μM vs 野生型8.7 μM),大幅提升抗原敏感性(图5);
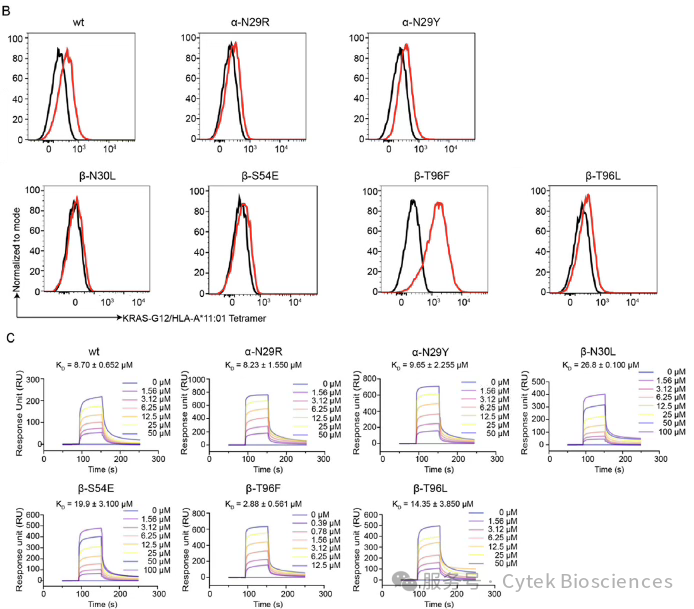
图5. 1–2C TCR 进行位点定向精细调节以增强结合和 T 细胞激活效力
-
晶体结构揭示突变增强范德华力(图6),且无脱靶毒性。
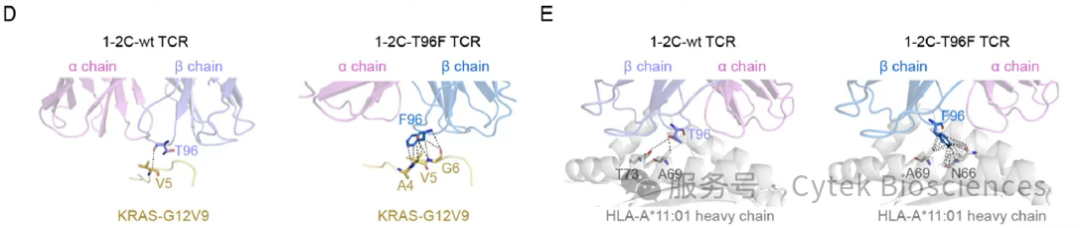
图6. 突变增强范德华力
3 强效抑瘤验证
-
在移植瘤模型中(SW-620-HLA-A11-Luci),高剂量组(10 mg/kg)显著抑制肿瘤生长(图7)。
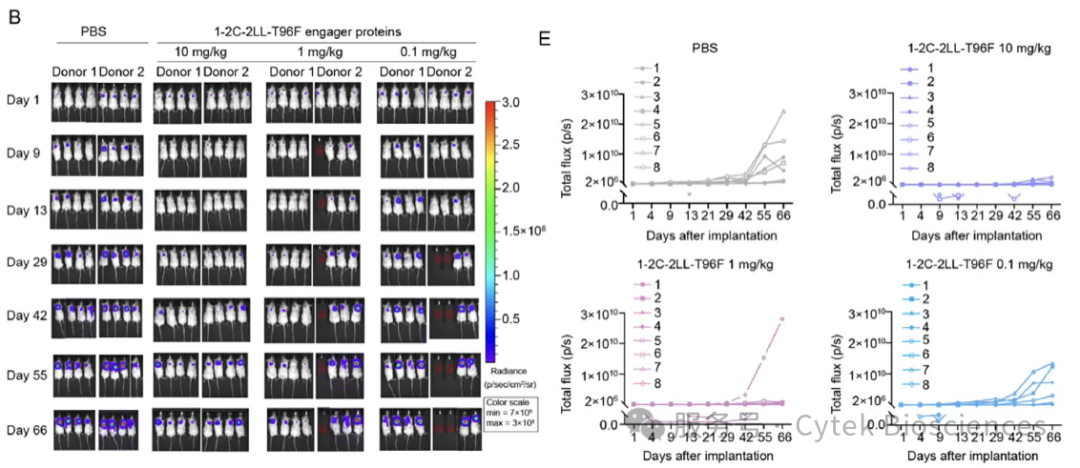
图7. T96F 突变的 1–2C-2LL在荷瘤小鼠模型中的抗肿瘤效果
Amnis®成像流式助力免疫突触检测!
免疫突触(immunological synapse)是T细胞与抗原呈递细胞(APC)或靶细胞相互作用时形成的特殊结构,对T细胞的激活、信号传导和免疫应答的启动起着关键作用。
文章中设计的可溶性 TCR 接合器旨在招募和重定向 T 细胞到肿瘤细胞附近,模拟自然的 TCR - pMHC 相互作用,促进免疫突触的形成,从而激活 T 细胞对肿瘤细胞的攻击。同时,免疫突触的形成影响 TCR engager 的效力,良好的免疫突触形成能够增强 T 细胞激活的信号强度和持续时间。
此外,TCR 与 pMHC 之间的结合亲和力以及 TCR 对特定抗原的特异性是影响免疫突触形成的关键因素,适当的结合亲和力能够保证 TCR 在遇到特定抗原时快速形成稳定的免疫突触。
最后,TCR engager 的结构稳定性也会影响其与 TCR 和 pMHC 的结合能力,进而影响免疫突触的形成,稳定的 TCR engager 能够更长时间地保持活性,促进免疫突触的形成和 T 细胞的激活。
关键环节—免疫突触形成验证,使用Amnis®成像流式技术实现可视化分析(图8)!
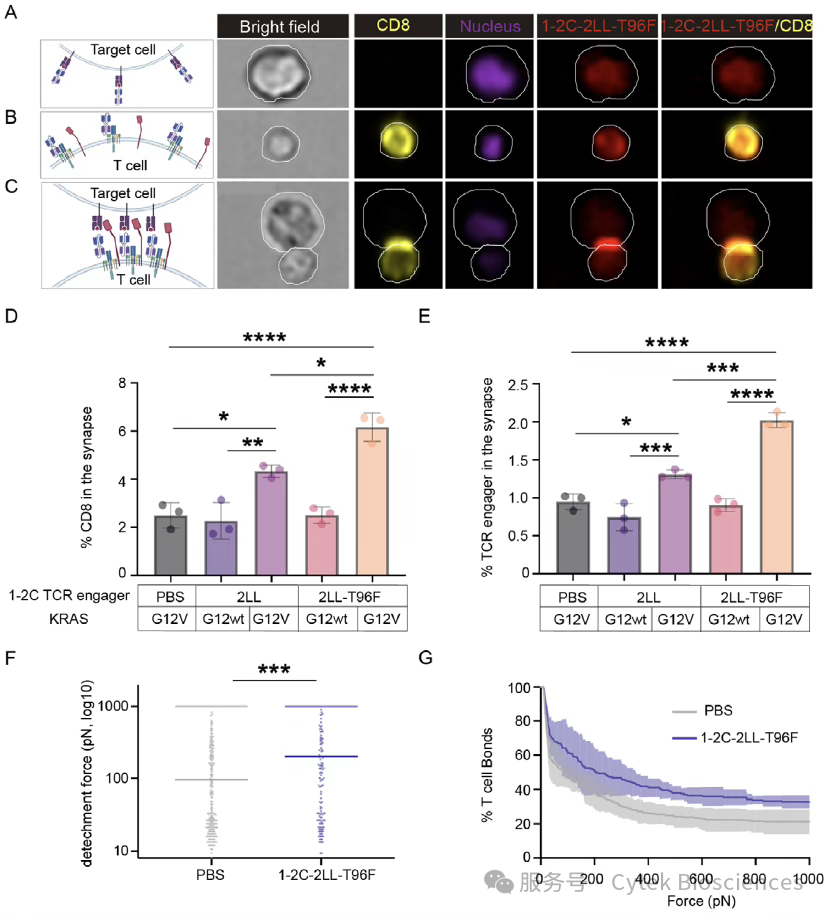
图8. Amnis®检测1–2C-2LL TCR接合器促进T细胞与靶细胞之间的免疫突触形成
成像流式实验设计
将T细胞、STanD-scTCR衔接器与负载KRAS-G12V肽的靶细胞共孵育,通过:
-
抗His标签抗体标记TCR衔接器(红色);
-
抗CD8抗体标记共受体(绿色);
-
Hoechst 33342 标记细胞核(蓝色)。
Amnis®成像流式检测免疫突触核心价值
免疫突触空间定位
-
清晰捕捉TCR衔接器与CD8分子在T细胞-靶细胞接触面的共聚集(图8A-C);
-
直观证实人工突触形成,模拟天然TCR-pMHC激活机制。
荧光强度定量分析
-
计算突触区域内外荧光强度比值,证明T96F突变显著提升CD8与TCR聚集效率(图8D-E);
-
定量数据为“突变增强T细胞活化”提供直接证据。
传统技术局限性 与Amnis®成像流式技术的突破
在免疫突触研究中,传统流式细胞术仅能分析表面标记分布,无法解析细胞接触界面的空间动态;共聚焦显微镜虽具备空间分辨率,却受限于低通量难以实现统计学验证;而静态成像技术则缺乏定量分析能力。
Amnis®成像流式技术一举突破三大瓶颈:其独有的空间分辨率可动态捕捉免疫突触形成过程(图8A-C),高通量特性支持单次分析数千细胞以获取统计学意义(图8D-E),更整合图像与荧光强度数据实现精准定量。
文章中这一技术优势转化为关键科学价值是不仅直接验证了STanD-scTCR衔接器诱导免疫突触的机制(图5),更通过量化突触区CD8共受体与TCR的聚集效率(图8D-E),为“T96F突变增强T细胞活化”的核心结论提供了不可替代的实验证据。
参考文献
Ma K, Wang J, Jiang M, He J, Li F, Lu D, Su C, Chai Y, Jin W, Chen Y, Zhang CWH, Ma X, Tan H, Gao GF, Tan S. An Engineered Soluble Single-Chain TCR Engager for KRAS-G12V Specific Tumor Immunotherapy. Adv Sci (Weinh). 2025






