Cytek Biosciences品牌商
7 年
手机商铺
- NaN
- 0
- 1
- 2
- 1
推荐产品
公司新闻/正文
全光谱流式纳米级维度分选——细胞外囊泡精准分选完整解决方案
521 人阅读发布时间:2025-09-04 15:19
研究背景
细胞外囊泡(EVs)属于细胞来源的膜包被纳米级颗粒,被释放到周围的环境中,尽管个头小,在临床诊断、药物递送、免疫治疗、再生医学等研究领域却是发挥着至关重要的作用。EVs粒径小且具有异质性,传统检测手段面临分辨率不足、灵敏度低等技术瓶颈,在精准识别与量化检测方面困难重重1。近些年来,单囊泡流式细胞术(vFC™)在众多检测平台中逐渐脱颖而出,其能够实现对EVs单颗粒的精准定量检测(图1)2, 3, 4。技术突破而探索不止,越来越多的研究人员也开始利用流式细胞分选仪对特异性EVs亚群进行精准分离,以深入解析其功能特性,并挖掘其在基础研究与临床治疗的应用潜力。
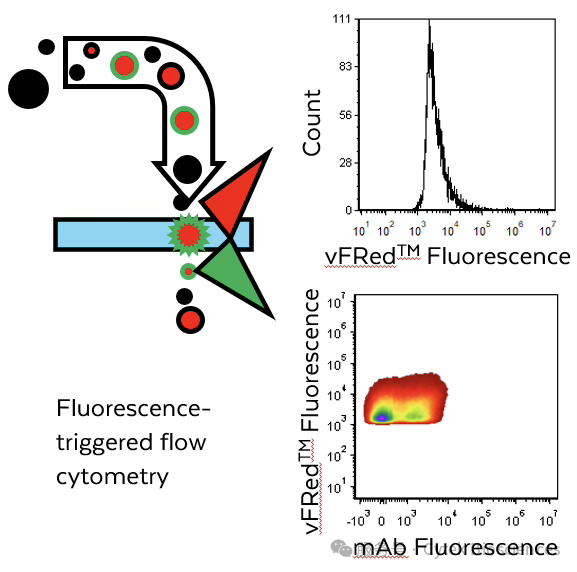
图1 – 单囊泡流式细胞术(vFC™)示例图
全光谱流式分选细胞外囊泡全流程
Cytek® Aurora™ CS全光谱流式分选仪作为全球首台搭载增强小颗粒(ESP™)检测模块的流式细胞分选仪,显著性提高了仪器灵敏度和分辨率,不仅能以“火眼金睛”识别EVs纳米级颗粒的完整发射光谱,还能成功分选特异性EVs,并对接下游功能性实验。2025年CYTO会议发表的一篇墙报备受关注,研究人员开创性地采用Cytek Aurora CS全光谱流式细胞仪分选EVs,从仪器设置、样本制备、试剂选择、数据分析等多维度构建了EVs分选的全流程实验体系。
1 仪器设置
研究人员基于5激光Cytek Aurora CS分选仪(搭载ESP检测模块),采用vCal nanoRainbow 微球(Cellarcus Biosciences)进行性能验证,并使用 vCal nanoCal 微球(Cellarcus Biosciences)和标记vFRed的合成囊泡尺寸标准品(Lipo100)进行仪器校准。软件中一键调取小颗粒检测默认增益(图2A),选择70 μm喷嘴及对应喷嘴优化条件(图2B)。
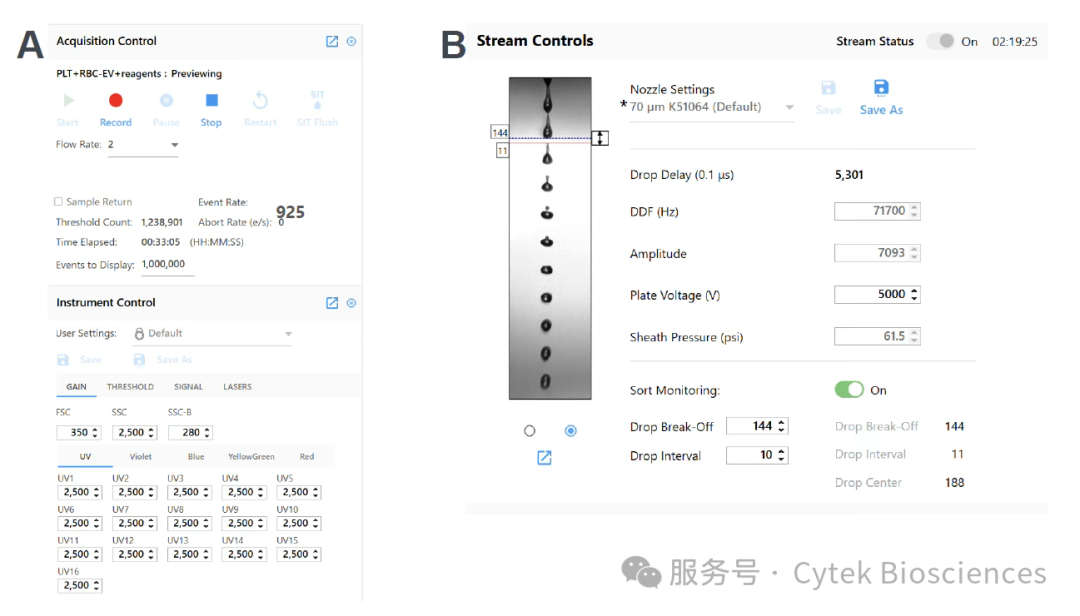
图2 – Cytek ESP检测模块仪器设置与70 μm喷嘴优化条件
2 样本制备
单标对照:vCal nanoCal 微球标记APC或BV421荧光抗体,EVs标记vFRed膜染料;
多标样品:血小板和红细胞来源的细胞外囊泡采用vFRed™ 染色标记膜包被颗粒,然后加入荧光抗体来特异性标记血小板(CD41-BV421)和红细胞来源EVs的表面标志物(CD235a-APC)。
3 门控策略
数据采集:对照管与样品管均采用低速获取2 min,控制采集速度以减少冲突事件发生,让双阳性门内细胞比例维持<0.5%(图3)。
遵循MIFlowCyt-EV指南要求,分选设门策略根据对照组(包括缓冲液组,缓冲液+试剂组,EVs+试剂组等)进行设置,从vFRed+门内区分出CD41+血小板来源EVs和CD235a+红细胞来源EVs(图3),采用多路分选模式,分别分选100万个颗粒到含有0.01%牛血清白蛋白的PBS缓冲液中。
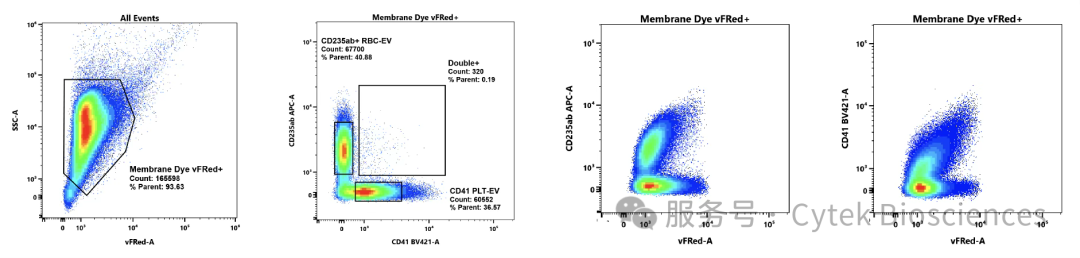
图3 - 血小板和红细胞来源的细胞外囊泡分选设门
4 分选回测
研究人员利用Cytek Aurora分析仪(与上述分选仪相同配置)对分选样品进行回测,两路分选纯度均高达97%以上。此外,分选报告显示,两路分选效率同样高达97%。采用vFRed染色的Lipo100囊泡尺寸标准品对分选到的EVs进行粒径校准,采用nanoCal 微球对其荧光单位(每个囊泡结合的抗体量,ABV)进行校准(图4)。
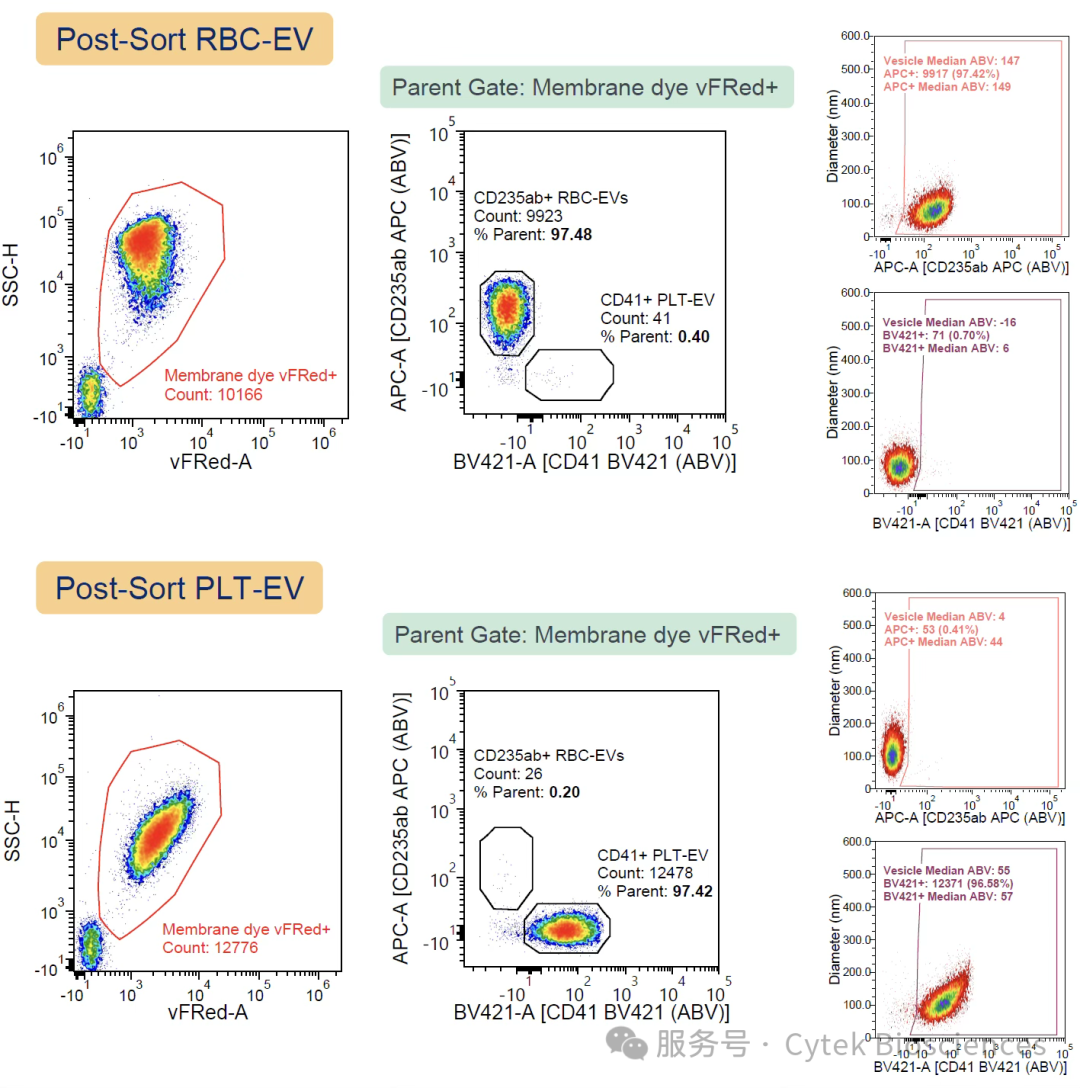
图4 – 搭载ESP检测模块的Cytek Aurora分析仪回测分选结果
总结展望
研究人员采用搭载ESP检测模块的Cytek Aurora CS分选仪,构建了基于表面标志物精准分选细胞外囊泡的全流程解决方案,回测实验充分证明了分选系统的卓越性能,为下游对接功能性实验提供了高质量的样本保障。Cytek Aurora CS 分选仪兼具精准分析与高效分选细胞外囊泡的功能,为纳米级颗粒研究开辟了新维度,加速了临床治疗和诊断开发的步伐。Cytek旗下的Cytek Aurora和 Cytek Northern Lights™ 全光谱流式分析仪、Cytek Aurora CS 全光谱流式分选仪均支持增强小颗粒 (ESP) 检测模块的全新配件,一机同时兼容小颗粒与大细胞的精准量化检测,成为科研人员和临床医生多样化场景实验需求标杆产品。

图5 – Cytek全光谱流式细胞仪在小颗粒领域潜力无限
参考文献
1 Welsh JA, et al. A compendium of single extracellular vesicle flow cytometry. Journal of Extracellular Vesicles. 2023 Feb;12(2):e12299.
2 Tekkatte C, et al. Identification of optimal conditions for human placental explant culture and extracellular vesicle release. iScience. 2023 Sep;26(10):108046.
3 Park DJ, et al. Defining the activity of pro-reparative extracellular vesicles in wound healing based on miRNA payloads and cell type-specific lineage mapping. Mol Ther. 2024.
4 Sandau US, et al. Methamphetamine use alters human plasma extracellular vesicles and their microRNA cargo: An exploratory study. Journal of Extracellular Vesicles. 2020 Nov;10(1):e12028.






